Protein
merupakan zat makanan yang sangat penting bagi tubuh karena berfungsi sebagai
sumber energi serta sebagai zat pembangun dan pengatur. Protein adalah polimer
dari asam amino yang dihubungkan dengan ikatan peptida. Molekul protein
mengandung unsur-unsur C, H, O, N, P, S, dan terkadang mengandung unsur logam
seperti besi dan tembaga.
Struktur asam amino digambarkan
sebagai berikut:
Protein yang
terdapat dalam bahan pangan mudah mengalami perubahan-perubahan, antara lain:
1.
Dapat terdenaturasi oleh perlakuan pemanasan.
2.
Dapat terkoagulasi atau mengendap oleh perlakuan pengasaman.
3.
Dapat mengalami dekomposisi atau pemecahan oleh enzim-enzim proteolitik.
4.
bisa bereaksi dengan gula reduksi, sehingga menyebabkan terjadinya warna coklat.
Analisis protein dalam bahan pangan dapat dilakukan
dengan dua metode yaitu metode
kuantitatif dan kualitatif.
Analisis protein secara kualitatif adalah analisis yang bertujuan untuk
mengetahui ada tidaknya protein dalam suatu bahan pangan. Dapat dilakukan
dengan reaksi Xantoprotein, reaksi Hopkins-Cole, reaksi Millon, reaksi
Nitroprusida dan reaksi Sakaguchi.
Sedangkan analisis protein secara kuantitatif adalah
analisis yang bertujuan untuk mengetahui kadar protein dalam suatu bahan
pangan. Analisi kuantitatif protein dapat dilakukan dengan metode Kjeldahl,
metode titrasi formol, metode Lowry, metode spektrofotometri visible (Biuret) dan
metode spektrofotometri UV. Analisis protein ini dapat menentukan tingkat
kualitas protein apabila dipandang dari sudut gizi serta menelaah protein yang
merupakan salah satu bahan kimia secara biokimia, fisiologis, reologis dan
enzimatis.
KJELDAHL
Metode Kjeldahl merupakan metode yang sederhana untuk penetapan nitrogen
total padaasam amino, protein dan senyawa yang mengandung nitrogen. Sampel
didestruksi denganasam sulfat dan dikatalisis dengan katalisator yang sesuai
sehingga akan menghasilkanamonium sulfat. Setelah pembebasan dengan alkali
kuat, amonia yang terbentuk disuling uapsecara kuantitatif ke dalam larutan
penyerap dan ditetapkan secara titrasi.
Metode ini telah banyak mengalami modifikasi. Metode
ini cocok digunakan secara semimikro, sebab hanyamemerlukan jumlah sampel dan
pereaksi yang sedikit dan waktu analisa yang pendek.Cara Kjeldahl digunakan untuk
menganalisis kadar protein kasar dalam bahan makanansecara tidak langsung,
karena yang dianalisis dengan cara ini adalah kadar nitrogennya.Dengan
mengalikan hasil analisis tersebut dengan angka konversi 6,25, diperoleh nilai
protein dalam bahan makanan itu.
|
No.
|
Nama bahan
|
Faktor konversi
|
|
1
|
Beer
|
6,5
|
|
2
|
Gandum
|
5,7
|
|
3
|
Roti
|
5,7
|
|
4
|
Syrup
|
6,25
|
|
5
|
Coklat
|
6,25
|
|
6
|
Serealia (biji-bijian)
|
6,25
|
|
7
|
SKM
|
6,25
|
|
8
|
yeast
|
6,25
|
|
9
|
Makanan ternak
|
6,25
|
|
10
|
Buah-buahan
|
6,25
|
|
11
|
Padi-padian
|
6,25
|
|
12
|
Makaroni/bakmi
|
5,7
|
|
13
|
Kacang-kacangan
|
6,25
|
|
14
|
Malt
|
6,25
|
|
15
|
The
|
6,25
|
|
16
|
Anggur
|
6,25
|
|
17
|
Wort (malt untuk beer)
|
6,25
|
Angka 6,25 berasal dari angka konversiserum albumin yang biasanya
mengandung 16% nitrogen.
Cara Kjeldahl pada umumnya dapat dibedakan atas dua cara, yaitucara makro
dan semimakro. Cara makro Kjeldahl digunakan untuk contoh yang sukar
dihomogenisasi dan besar contoh 1-3 g, sedang semimikro Kjeldahl dirancang
untuk contohukuran kecil yaitu kurang dari 300 mg dari bahan yang homogen. Cara
analisis tersebut akan berhasil baik dengan asumsi nitrogen dalam bentuk ikatan
N-N dan N-O dalam sampel tidak terdapat dalam jumlah yang besar.
Analisa
protein metode Kjeldahl pada dasarnya dapat dibagi menjadi tiga tahapan yaitu :
1. Tahap destruksi
Pertama,
sampel dipanaskan dalam H2SO4 pekat sehingga terjadi
destruksi menjadi unsur-unsurnya. Elemen karbon, hidrogen teroksidasi menjadi
CO, CO2 dan H2O. Sedangkan nitrogennya (N) akan berubah
menjadi (NH4)2SO4. Untuk mempercepat proses destruksi
sering ditambahkan katalisator berupa campuran Na2SO4 dan
HgO (20:1). Gunning menganjurkan menggunakan K2SO4 atau
CuSO4. Dengan penambahan katalisator tersebut titk didih H2SO4akan
dipertinggi sehingga destruksi berjalan lebih cepat. Selain katalisator yang
telah disebutkan tadi, kadang-kadang juga diberikan Selenium. Selenium dapat
mempercepat proses oksidasi karena zat tersebut selain menaikkan titik didih
juga mudah mengadakan perubahan dari valensi tinggi ke valensi rendah atau
sebaliknya.
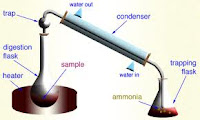
2. Tahap destilasi
Pada tahap ini, ammonium
sulfat dipecah menjadi ammonia (NH3) dengan penambahan NaOH sampai
alkalis dan dipanaskan. Agar selama destilasi tidak terjadi superheating
ataupun pemercikan cairan atau timbulnya gelembung gas yang besar maka dapat
ditambahkan logam zink (Zn). Ammonia yang dibebaskan selanjutnya akan ditangkap
oleh asam khlorida atau asam borat 4 % dalam jumlah yang berlebihan. Agar
supaya kontak antara asam dan ammonia lebih baik maka diusahakan ujung tabung
destilasi tercelup sedalam mungkin dalam asam. Untuk mengetahui asam dalam
keadaan berlebihan maka diberi indikator misalnya BCG + MR atau PP.
3. Tahap
titrasi
Apabila penampung destilat
digunakan asam khlorida maka sisa asam khorida yang bereaksi dengan ammonia
dititrasi dengan NaOH standar (0,1 N). Akhir titrasi ditandai dengan tepat
perubahan warna larutan menjadi merah muda dan tidak hilang selama 30 detik
bila menggunakan indikator PP.
%N = × N. NaOH × 14,008 × 100%
Apabila penampung destilasi
digunakan asam borat maka banyaknya asam borat yang bereaksi dengan ammonia
dapat diketahui dengan titrasi menggunakan asam khlorida 0,1 N dengan indikator
(BCG + MR). Akhir titrasi ditandai dengan perubahan warna larutan dari biru
menjadi merah muda.
%N = × N.HCl × 14,008 × 100 %
Setelah diperoleh %N, selanjutnya
dihitung kadar proteinnya dengan mengalikan suatu faktor. Besarnya faktor
perkalian N menjadi protein ini tergantung pada persentase N yang menyusun
protein dalam suatu bahan.
Keuntungan dari metode kjedahl :
• Metode Kjeldahl digunakan secara luas di seluruh
dunia dan masih merupakan metode standar dibanding metode lain.
• Sifatnya yang universal, presisi tinggi dan
reprodusibilitas baik membuat metode ini banyak digunakan untuk penetapan kadar
protein dalam makanan.
• Metode ini tidak memberikan pengukuran protein
sesungguhnya, karena tidak semua nitrogen dalam makanan bersumber dari protein,
yaitu purina, pirimidina, vitamin-vitamin,
asam amino besar, kreatina, dan kreatinina ikut teranalisis danterukur sebagai
nitrogen protein.
• Protein yang berbeda memerlukan faktor koreksi yang
berbeda karena susunan residu asam amino yang berbeda.
• Penggunaan asam sulfat pada suhu tinggi berbahaya,
demikian juga beberapa katalis.
• Teknik ini membutuhkan waktu lama.
daftar pustaka:
rinaherowati.files.wordpress.com/2011/10/2-analisis-protein_.pdf